 | Главная :: Архив статей :: Поиск :: Гостевая :: Внешняя :: Ссылки |
Архив статей > Химия > Лантаноиды
Лантаноиды
В. В. Станцо
Химия и Жизнь №12, 1971 г., с. 39-45
ГАДОЛИНИЙ
Элемент № 64 - гадолиний открыт в 1880 году. Первооткрыватель этого элемента - швейцарский химик Жан Шарль Галиссар де Мариньяк (1817-1894) долгое время работал во Франции. Общие научные интересы - редкие земли и спектральный анализ - сблизили его с Лекок де Буабодраном. Именно Лекок де Буабодран, с согласия Мариньяка, назвал гадолиниевой открытую им новую землю. А через два года после смерти Мариньяка был впервые получен в относительно чистом виде элементарный гадолиний. Между прочим, это был первый случай в истории науки, когда химический элемент назвали в память об ученом, члене-корреспонденте Петербургской академии - Юхане Гадолине, который был одним из первых исследователей редких земель.
На первый взгляд, по физическим и химическим свойствам гадолиний ничем не отличается от других редкоземельных металлов. Он - светлый, незначительно окисляющийся на воздухе металл - по отношению к кислотам и другим реагентам ведет себя так же, как лантан и церий. Но с гадолиния начинается иттриевая подгруппа редкоземельных элементов, а это значит, что на электронных оболочках его атомов должны быть электроны с антипараллельными спинами.
Всего один дополнительный электрон появился в атоме гадолиния по сравнению с атомом предыдущего элемента самария. Он, этот добавочный электрон, попал на вторую снаружи оболочку, а первые пять электронных "слоев", в том числе и развивающаяся у большинства лантаноидов оболочка N, у атомов самария и гадолиния построены одинаково. Всего один электрон и один протон в ядре, но как преображают они некоторые свойства очередного лантаноида!
Прежде всего гадолинию свойственно наивысшее среди всех элементов сечение захвата тепловых нейтронов, 46000 барн - такова эта величина для природной смеси изотопов гадолиния. А у гадолиния-157 (его доля в природной смеси - 15,68%) сечение захвата превышает 150000 барн. Гадолиний-157 - "рекордсмен" среди всех стабильных изотопов.
Отсюда возможности гадолиния при управлении цепной ядерной реакцией и для защиты от нейтронов. Правда, активно захватывающие нейтроны изотопы гадолиния, 157Gd и 155Gd, в реакторах довольно быстро "выгорают" - превращаются в "соседние" ядра, у которых сечение захвата на много порядков меньше. Поэтому в конструкциях регулирующих стержней с гадолинием могут конкурировать другие редкоземельные элементы, прежде всего самарий и европий.
Но не только рекордными сечениями захвата знаменит гадолиний. У него наибольшее из всех лантаноидов удельное электрическое сопротивление - примерно вдвое больше, чем у его аналогов. Почти в два раза больше, чем у лантана и церия, и удельная теплоемкость гадолиния. Наконец, магнитные свойства ставят элемент № 64 в один ряд с железом, кобальтом и никелем. В то время как лантан и другие лантаноиды парамагнитны, гадолиний - ферромагнетик, причем даже более сильный, чем никель и кобальт. Но железо и кобальт сохраняют ферромагнитность и при температурах порядка 1000°С, никель - до 63°С. Гадолиний же теряет это свойство, будучи нагрет всего до 290°С.
Необычны магнитные свойства и у некоторых соединений гадолиния. Его сульфат и хлорид (гадолиний, кстати, всегда трехвалентен), размагничиваясь, заметно охлаждаются. Это свойство использовали для получения сверхнизких температур. Сначала соль состава Gd2(SO4)3·8H2O помещали в магнитное поле и охлаждали до предельно возможной температуры. А затем давали ей размагнититься. При этом запас энергии, которой обладала соль, еще уменьшался, и в конце опыта температура кристаллов от абсолютного нуля отличалась всего на одну тысячную градуса.
Жан Шарль Галиссар де Мариньяк (1817-1894) - швейцарский химик, первооткрыватель гадолиния
Сверхнизкие температуры открыли еще одно применение элементу № 64. Сплав гадолиния с церием и рутением в этих условиях приобретает сверхпроводимость. И в то же время в нем наблюдали слабый ферромагнитизм. Таким образом, для магнетохимии представляют непреходящий интерес и сам гадолиний, и его соединения,и сплавы.
Другой сплав гадолиния - с титаном - применяют в качестве активатора в стартерах люминесцентных ламп. Этот сплав впервые получен в нашей стране.
Несколько слов о других практически важных соединениях элемента № 64. Окись гадолиния Gd2O3 используют как один из компонентов железо-иттриевых ферритов. Новый люминофор - оксисульфид гадолиния Gd2O2S позволяет получить более контрастные рентгеновские снимки. Молибдат гадолиния - компонент галлий-гадолиниевых гранатов. Эти материалы представляют большой интерес для оптоэлектроники.
Вероятно, заканчивая, следует указать цены на гадолиний. Этот своеобразный элемент достаточно дорог. В 1970 году килограмм гадолиния чистотой 99,76% стоил 1500 рублей. Это, конечно, дорого. Гадолиний, однако, дешевле, чем европий, тербий, лютеций, тулий. Дешевле, чем золото и платина. Но дороже, чем серебро.
ТЕРБИЙ
Элемент № 65. В природе существует в виде одного-единственного стабильного изотопа тербий-159. Элемент редкий, дорогой и используемый пока в основном для изучения свойств элемента № 65. Весьма ограниченно соединения тербия используют в люминофорах, лазерных материалах и ферритах.

Французский химик Жорж Урбен (1872-1938), первым получивший чистые препараты тербия, первооткрыватель лютеция.
Тербий - идеальный парамагнетик. В чистом виде представляет собой металл серебристого цвета, который при нагревании покрывается окисной пленкой.
Темно-коричневый порошок окиси тербия имеет состав Тb4О7 или Тb2О3·2ТbО2. Это значит, что при окислении часть атомов тербия отдает по три электрона, а другая часть - по четыре, Треххлористый тербий ТbСl3 - самое легкоплавкое соединение из всех галогенидов редкоземельных элементов - плавится при температуре меньше 600°С.
История тербия достаточно путаная. В течение полувека существование этого элемента не раз брали под сомнение, несмотря на то что первооткрывателем тербия был такой авторитет в химии редких земель, как Карл Мозандер. Это он разделил в 1843 году иттриевую землю на три: иттриевую (белого цвета), тербиевую (коричневого) и эрбиевую (розового). Но такие известные ученые XIX века, как Р. Бунзен и Т. Клеве, нашли в иттриевой земле лишь два окисла и считали сомнительным существование третьей - тербиевой земли. Позже Лекок де Буабодран обнаружил тербий (вместе с гадолинием и самарием) в псевдоэлементе мозандрии. Однако затем он сам запутался, придя к выводу, что существует не один тербий, а несколько элементов - целая группа тербинов... Словом, путаницы было хоть отбавляй. И лишь в начале XX века известный французский химик Жорж Урбен (1872-1938) получил чистые препараты тербия и положил конец спорам.
ДИСПРОЗИЙ
Диспрозий - один из самых распространенных элементов иттриевой подгруппы. В земной коре его в 4,5 раза больше, чем вольфрама. Выглядит он так же, как и остальные члены редкоземельного семейства, проявляет валентность 3+; окраска окиси и солей светло-желтая, обычно с зеленоватым, реже с оранжевым оттенком.
Название этого элемента происходит от греческого dusprositoV, что означает "труднодоступный". Название элемента № 66 отразило трудности, с которыми пришлось столкнуться его первооткрывателю. Окисел этого элемента - "землю" диспрозия открыл Лекок де Буабодран спектроскопически, а затем выделил ее из окиси иттрия. Произошло это в 1886 году, а через 20 лет Жорж Урбен получил диспрозий в относительно чистом виде.
Среди прочих лантаноидов диспрозий мало чем выделяется. Правда, ему, как и гадолинию, при определенных условиях свойствен ферромагнетизм, но только при низких температурах. Специалисты видят в диспрозии ценный компонент сплавов со специальными магнитными свойствами.
Для атомной энергетики диспрозий представляет ограниченный интерес, по-скольку сечение захвата тепловых нейтронов у него достаточно велико (больше 1000 барн) по сравнению с бором или кадмием, но намного меньше, чем у некоторых других лантаноидов - гадолиния, самария... Правда, диспрозий более тугоплавок, чем они, и это в какой-то мере уравнивает шансы.
ГОЛЬМИЙ
На VIII Менделеевском съезде (1958 год) выступил известный немецкий ученый, один из первооткрывателей рения, Вальтер Ноддак. Но не рению был посвящен его доклад. "Техническое разделение и получение в чистом виде редкоземельных элементов семейства иттрия" - так была сформулирована тема. Ноддак рассказал, в частности, что ему пришлось проделать 10000 фракционных кристаллизации для того, чтобы выделить 10 миллиграммов чистой окиси гольмия... Сейчас методами жидкостной экстракции и ионного обмена получают сотни килограммов окиси гольмия чистотой более 99,99%.
Для соединений элемента № 67, элемента рассеянного и редкого, характерна желтая окраска различных оттенков. Пока эти соединения используют только в исследовательских целях. Правда, несколько лет назад в печати промелькнуло сообщение, что ион Но3+ может быть использован для возбуждения лазерного излучения в инфракрасной области (длина волны 2,05 микрона). Но подобными же свойствами обладают ионы других лантаноидов - разница лишь в длине излучаемых волн.
Гольмий - идеальный парамагнетик, но подобные магнитные свойства у большинства редкоземельных элементов.
Моноизотопность природного гольмия (весь он состоит из атомов с массовым числом 165) тоже не делает элемент №67. уникальным. Установлено, что соединения гольмия можно использовать в качестве катализаторов, но и другим лантаноидам свойственна каталитическая активность... Таким образом, получается, что пока элемент № 67 "не нашел своего лица"...
Как считают большинство историков науки, гольмий открыт шведским химиком Т. П. Клеве в 1879 году. Клеве, продолжая разделять компоненты окиси иттрия, выделил из окиси эрбия аналогичные соединения иттербия, тулия и гольмия. Правда, в те же годы (1878-1879) швейцарец Сорэ исследовал спектры эрбиевой земли и обнаружил раздвоение некоторых спектральных линий. Он обозначил новый элемент индексом X; теперь известно, что найденные им новые линии принадлежат гольмию. Название элементу № 67 дал Клеве: Holmia - так пишется по латыни старинное название Стокгольма.
ЭРБИЙ
Окись эрбия Карл Мозандер выделил из иттриевой земли в 1843 году. Впоследствии эта розовая окись стала источником, из которого "почерпнули" еще два новых редкоземельных элемента - иттербий и тулий.
Кроме розовой окраски большинства соединений, в том числе окиси Еr2О3, эрбий почти ничем не отличается от прочих лантаноидов иттриевой подгруппы. Пожалуй, лишь несколько большие прочность и твердость выделяют этот элемент среди других лантаноидов.
Вместе с лютецием и тулием эрбий принадлежит к числу самых тяжелых лантаноидов - его плотность больше 9 г/см3.
Основная область применения эрбия сегодня - это изготовление сортового окрашенного стекла. Кроме того, стекла, в составе которых есть эрбий, отлично поглощают инфракрасные лучи.
В числе потенциальных областей применения элемента № 68 атомная энергетика (регулирующие стержни), светотехника (активатор фосфоров), производство ферритов и магнитных сплавов, лазеры. Здесь уже используют окись эрбия с примесью тулия.
ТУЛИЙ
Thule - так во времена римской империи называли Скандинавию - север Европы. Тулием назван элемент, открытый Т. П. Клеве в 1879 году. Сначала Клеве нашел новые спектральные линии, он же первым выделил из гадолинита бледно-зеленую окись элемента № 69.

Т. П. Клеве (1840-1905) - шведский химик, геолог и ботаник, первооткрыватель тулия и гольмия.
По данным академика А. П. Виноградова, тулий - самый редкий (если не считать прометия) из всех редкоземельных элементов. Содержание его в земной коре 8·10-5%. По тугоплавкости тулий второй среди лантаноидов: температура его плавления 1550-1600°С (в разных справочниках приводятся разные величины; дело, видимо, в неодинаковой чистоте образцов). Лишь лютецию уступает он и по температуре кипения.
Несмотря на минимальную распространенность, тулий нашел практическое применение раньше, чем многие более распространенные лантаноиды. Известно, например, что микропримеси тулия вводят в полупроводниковые материалы (в частности, в арсенид галлия) и в материалы для лазеров. Но, как это ни странно, важнее, чем природный стабильный тулий (изотоп 169Тm), для нас оказался радиоактивный тулий-170.
Тулий-170 образуется в атомных реакторах при облучении нейтронами природного тулия. Этот изотоп с периодом полураспада 129 дней излучает сравнительно мягкие гамма-лучи с энергией 84 Кэв (энергия жесткого гамма-излучения измеряется не килоэлектрон-вольтами, а Мэвами - миллионами злектрон-вольт).
На основе этого изотопа были созданы компактные рентгено-просвечивающие установки, имеющие массу преимуществ перед обычными рентгеновскими аппаратами. В отличие от них тулиевые аппараты не нуждаются в электропитании, они намного компактнее, легче, проще по конструкции. Миниатюрные тулиевые приборы пригодны для рентгенодиагностики в тех тканях и органах, которые трудно, а порой невозможно, просвечивать обычными рентгеновскими аппаратами.

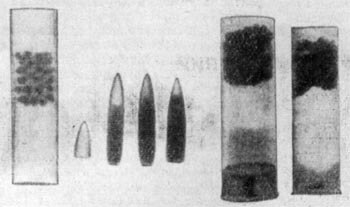
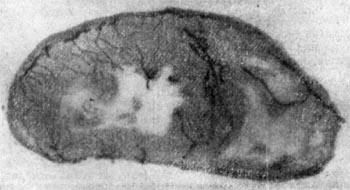
Эти фотографии получены при помощи гамма-излучения изотопа тулий-170. На снимке фотокамеры видны тончайшие пластмассовые и металлические детали; внутреннее строение пуль и патронов - как на ладони; внизу гамма-снимок кровеносных сосудов, заполненных контрольным веществом
Гамма-лучами тулия просвечивают не только живые ткани, но и металл. Тулиевые гамма-дефектоскопы очень удобны для просвечивания тонкостенных деталей и сварных швов. При работе с образцами толщиной не больше б мм эти дефектоскопы наиболее чувствительны. С помощью тулия-170 были обнаружены совершенно незаметные письмена и символические знаки на бронзовой прокладке ассирийского шлема IX века до н. э. Шлем обернули фотопленкой и стали просвечивать изнутри мягкими гамма-лучами тулия. На проявленной пленке появились стертые временем знаки...
Препараты тулия-170 используют также в приборах, называемых мутнометрами. Этими приборами определяют количество взвешенных частиц в жидкости по рассеянию в ней гамма-лучей. Такие приборы используют при строительстве гидротехнических сооружений.
Для тулиевых приборов характерны компактность, надежность, быстродействие. Единственный их недостаток - сравнительно малый период полураспада тулия-170. Но тут уж, как говорится, ничего не попишешь.
Тулиевые гамма-источники становятся дешевле по мере увеличения их производства. Еще в 1961 году в нашей стране выпускались тулиевые источники пяти типов и стоили они от 5,5 до 250 рублей. А килограмм металлического стабильного тулия в то же время стоил более 25000 рублей. Новая более совершенная технология получения лантаноидов позволила в последнее время значительно уменьшить цены. В 1970 году цена тулия составляла уже лишь 13000 рублей за килограмм. Став почти вдвое дешевле, он по-прежнему остается самым редким и самым дорогим из всех лантаноидов.
ИТТЕРБИЙ
И снова элемент, о котором почти нечего рассказывать. Если шведскому местечку Иттербю повезло в том смысле, что его название запечатлелось в именах четырех химических элементов, то сами эти элементы, исключая иттрий, можно отнести к разряду наименее интересных. Иттербию, правда, свойственны некоторые отклонения от редкоземельного стандарта. В частности, он способен проявлять валентность 2+, это помогает выделить иттербий.
Из всех лантаноидов он больше всего похож на европий: малые атомный объем и атомный радиус, пониженные (по сравнению с другими лантаноидами) плотность и температура плавления - все это свойственно европию и иттербию. Зато электропроводность у иттербия почти втрое больше, чем у других лантаноидов, включая европий.
Окись иттербия и его соли белого цвета.
Практическое применение этого элемента ограничено некоторыми специальными сплавами, в основном на алюминиевой основе. Кроме того, смесь окислов иттербия и иттрия добавляют в огнеупоры на основе двуокиси циркония. Такая добавка стабилизирует свойства огнеупоров.
ЛЮТЕЦИЙ
А это старушка, седая и строгая,
Которая доит корову безрогую.
Лягнувшую старого пса без хвоста,
Который за шиворот треплет кота,
Который пугает и ловит синицу,
Которая часто ворует пшеницу.
Которая в темном чулане хранится,
В доме, Который построил Джек.
Эти детские стихи приходят на память, когда пытаешься коротко пересказать историю открытия элемента № 71 - лютеция. Судите сами:
новая редкоземельная окись - лютеция
выделена Жоржем Урбеном в 1907 году из иттербиевой земли,
которая в 1878 году выделена Мариньяком из эрбиевой земли,
которая в 1843 году выделена Мозандером из иттриевой земли,
которая открыта Экебергом в 1797 году в минерале гадолините.
Название нового элемента Урбен произвел от старинного латинского названия столицы Франции Парижа (видимо, в противовес гольмию).
Приоритет Урбена оспаривал Ауэр фон Вельсбах, который открыл элемент № 71 несколькими месяцами позже и назвал его кассиопеем. В 1914 году Международная комиссия по атомным весам вынесла решение именовать элемент все-таки лютецием, но еще много лет в литературе, особенно немецкой, фигурировало название "Кассиопей".
Лютеций - последний лантаноид, самый тяжелый (плотность 9,849 г/см3), самый тугоплавкий (температура плавления 1700±50°С), самый, пожалуй, труднодоступный и один из самых дорогих (12000 рублей за килограмм - цена 1970 года). В полном соответствии с правилом лантаноидного сжатия атом лютеция имеет наименьший среди всех лантаноидов объем, а ион Lu3+ - минимальный радиус, всего 0,99 А. По остальным же характеристикам и свойствам лютеций мало отличается от других лантаноидов.
Природный лютеций состоит всего из двух изотопов - стабильного лютеция-175 (97,412%) и бета-активного лютеция-176 (2,588%) с периодом полураспада 20 миллиардов лет. Так что за время существования нашей планеты количество лютеция слегка уменьшилось. Искусственным путем получены еще несколько радиоизотопов лютеция с периодами полураспада от 22 минут до 500 дней. Последний изотоп лютеция (нейтронно-дефицитный, с массовым числом 166) получен в 1968 году в Дубне.
Практического значения элемент №71 пока не имеет. Известно, однако, что добавка лютеция положительно влияет на свойства хрома. Не исключено, что, по мере того как лютеций будет становиться доступнее, его удастся использовать как катализатор или как активатор люминофоров или в лазерах - одним словом, там, где успешно работают его "собратья" по лантаноидной "команде".
Вот и закончены рассказы о лантаноидах - элементах, которым всем без исключения прочат большое будущее. Как говорится, поживем - увидим, но для оптимизма есть основания. Если бы Мариньяку, Лекок де Буабодрану, Клеве, Ауэру фон Вельсбаху, Демарсэ и другим выдающимся исследователям редких земель, жившим в конце XIX - начале XX века, сказали, что во второй половине XX века открытые ими элементы станут важны для техники, первооткрыватели, наверное, не поверили бы этому утверждению. Кроме, может быть, Урбена - он ведь был не только химиком, но и художником...
Главная :: Архив статей :: Поиск :: Гостевая :: Внешняя :: Ссылки
Помоги сайту! Брось денежку в смс-копилку!